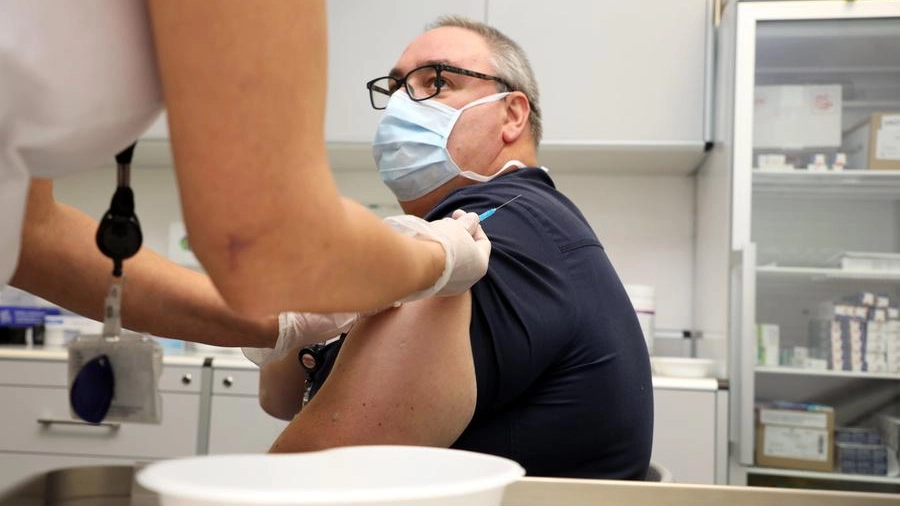
E' corsa ai vaccini anti-Covid (Imagoeconomica)
L’Agenzia europea per i medicinali (Ema) potrebbe pronunciarsi a fine mese riguardo la richiesta di autorizzazione condizionata all’impiego nell’Unione Europea del vaccino Oxford/AstraZeneca, realizzato con vettore virale innocuo. Questo il cronoprogramma ipotizzato dai vertici dell’Agenzia regolatoria alla luce dei dati supplementari di efficacia della profilassi introdotti nel dossier già consegnato. All’Italia entro marzo spettano 16 milioni di fiale.
Vaccinati italiani: la dashboard in tempo reale
Covid, il bollettino del 9 gennaio
Intanto i negoziatori Ue, che avevano concordato una prima fornitura di 300 milioni di dosi del vaccino Pfizer, hanno deciso di estendere quel contratto in modo da acquistare "altre 300 milioni di somministrazioni aggiuntive, raddoppiando la disponibilità iniziale". L’ha annunciato Ursula von der Leyen, presidente della Commissione. All’Italia dovrebbe andare il 13,5% del nuovo lotto di vaccini, pari a 40,5 milioni di dosi, per un totale di 81 milioni entro fine anno.
Il Regno Unito ha validato intanto il siero Moderna, mentre l’Oms ha deplorato la politica degli accordi bilaterali tra aziende farmaceutiche e singoli governi, perché privilegia le nazioni economicamente forti. "Alla disponibilità dei primi due vaccini già approvati - dichiara Pierpaolo Sileri, viceministro della Salute - dobbiamo aggiungerere quelli degli altri produttori, una volta autorizzati. Con quelli che abbiamo al momento possiamo immunizzare solo il 20% della popolazione prima dell’estate".
In Europa il via libera al primo vaccino anti Covid-19, sviluppato da BioNTech e Pfizer, è arrivato il 22 dicembre scorso. Gli operatori sanitari sottoposti per primi alla profilassi (medici e infermieri) sono quelli destinati, a loro volta, a praticare le vaccinazioni a strati sempre più ampi di popolazione. Il vaccino Pfizer BioNTech prevede due somministrazioni a distanza di 21 giorni una dall’altra. L’immunità si produce progressivamente e si considera pienamente acquisita una settimana dopo la seconda iniezione. Questo vaccino va conservato in azoto liquido a meno i 70°, una volta portato a temperatura ambiente viene inoculato con una semplice intramuscolo in maniera indolore. Questo vaccino utilizza la tecnologia mRNA.
Come funzionano i diversi vaccino) Che efficacia hanno? Ecco la guida per orientarsi: domande e risposte.
1) Pfizer, quando scatta la protezione?
L’industria farmaceutica ha riprodotto in laboratorio sequenze di codice che, opportunamente veicolate nelle cellule umane, fungono da messaggeri e riproducono parti della proteina virale (spike). Queste vengono riconosciute come ostili dal sistema immunitario, tanto da stimolare le difese naturali del nostro organismo, inducendole a fabbricare anticorpi neutralizzanti contro il virus Sars-Cov-2.
2) Che efficacia ha Moderna sugli over 65?
L’Agenzia italiana del farmaco ha dato l’ok al vaccino Moderna mRNA-127 per la prevenzione della malattia da Coronavirus sottolineando che in termini di efficacia e sicurezza questo appare sovrapponibile al primo vaccino anti Covid-19 sviluppato da BioNTech e Pfizer. Franco Locatelli, presidente del Consiglio superiore di sanità (Css), alla conferenza stampa al ministero della Salute sull’analisi dei dati del monitoraggio regionale della cabina di regia, ha detto che i dati sul siero Moderna mostrano percentuali di efficacia sopra l’85% nei soggetti ultra65enni. Riferendosi al profilo di sicurezza del vaccino (che si conserva più facilmente in frigorifero, ndr) ha aggiunto che è assolutamente in linea con quello osservato con Pfizer.
3) Quando arriverà la profilassi Curevac?
C’è assoluto bisogno di vaccini in quantità industriali. Per questo la Commissione europea ha firmato un contratto di fornitura, cooperazione e service, finalizzato all’acquisto di 405 milioni di dosi da Curevac, una start up europea con sede a Tubinga che impiega tecnologie a Rna messaggero, le stesse adottate da Pfizer e da Moderna. I laboratori CureVac contano di arrivare entro fine anno a produrre il vaccino contro il Covid-19, hanno lanciato a dicembre la terza e ultima fase delle sperimentazioni e hanno stretto con Bayer un accordo per essere supportati al fine di ottenere l’approvazione e avviare la produzione.
4) Con ReiThera ci basterà solo una dose?
ReiThera è un vaccino sperimentale concepito e realizzato in Italia. Giuseppe Ippolito, direttore scientifico dell’Istituto Spallanzani di Roma, ha dichiarato che «il 92,5% dei vaccinati ha sviluppato anticorpi rilevabili con una sola dose. Comparando i dati di questo studio con Moderna e Pfizer siamo in linea, e ci aspettiamo la capacita del vaccino di prevenire la malattia sostanzialmente come gli altri sieri. L’ ipotesi è di chiudere i test clinici di fase 3 entro l’estate». Se le prove di efficacia e sicurezza proseguiranno secondo tali premesse, la profilassi ReiThera potrebbe essere sottoposta all’esame delle agenzie regolatorie in tempi relativamente brevi, per poi andare a integrarsi con gli altri sieri già in produzione.
5) Lo Sputnik funziona veramente?
Si fa strada anche in America latina il vaccino russo Sputnik V. Il ministro della Salute argentino, Ginés González García, ha riferito che a fronte delle prime trentamila vaccinazioni, che hanno riguardato prioritariamente il personale sanitario nel paese, realizzate tutte con il vaccino russo Sputnik V, si sono registrati solo 317 eventi avversi, di cui il 99,3% classificati come reazioni lievi o moderate. Intervenendo nella polemica suscitata a Buenos Aires sulla sicurezza del siero prodotto dal laboratorio russo Gamaleya, García ha sottolineatoche «la presenza di febbre, cefalea o dolori muscolari, come sintomi unici o associati, ha riguardato l’80% degli eventi registrati, e che questi sono pari all’1 per cento di tutte le somministrazioni». Parliamo di un vaccino efficace, nel quale il virus patogeno è assente. Sputnik V impiega infatti un frammento di adenovirus umano ricombinante che ingloba un antigene derivato dal virus Sars-Cov-2 capace di stimolare la produzione di anticorpi neutralizzanti.

